É notório que existe um claro movimento no sentido de melhorar a qualidade do diagnóstico laboratorial no setor agropecuário do Brasil. Porém, ainda há carência de legislações mais abrangentes e mais duráveis para dar ao setor maior segurança. Agora que os laboratórios credenciados pelo MAPA já estão acreditados, sendo avaliados regular e periodicamente pela Coordenação Geral de Acreditação do INMETRO, são necessários outros avanços no sentido de tornar o diagnóstico mais confiável.
Qualidade em laboratório deve ser entendida como uma série de procedimentos ajustados para garantir a confiabilidade e consistência dos resultados. A acreditação dos laboratórios veterinários por organismos que atestam a conformidade e possuem autoridade para realizar acreditação como o Instituto Nacional de Metrologia, Normalização e Qualidade Industrial – INMETRO tem, dentre outros, o objetivo de fortalecer as empresas nacionais, aumentando sua produtividade por meio da adoção de mecanismos destinados à melhoria da qualidade dos serviços prestados. A acreditação provê confiança à sociedade em relação aos ensaios, padroniza os procedimentos em todo o território nacional e promove harmonização das relações de consumo, a inovação e a competitividade do país e, principalmente fortalece a participação do Brasil nas atividades internacionais relacionadas à sanidade animal. A acreditação é voluntária, mas no caso da participação de laboratórios nos programas nacionais de sanidade animal se tornou compulsória. Ou seja, para que o laboratório se credencie e participe da Rede Nacional de Laboratórios Agropecuários (RNLA) do Sistema Unificado de Atenção à Sanidade Agropecuária, é exigido o certificado de acreditação emitido pela Coordenação Geral de Acreditação-CGCRE/INMETRO.
Há alguns anos percebe-se um movimento claro de melhoria da qualidade do diagnóstico laboratorial dando maior credibilidade nacional e internacional aos processos relacionados à defesa agropecuária do Brasil. A Instrução Normativa n° 24 de 27/06/2001 já apontava para a exigência de um sistema da qualidade nos laboratórios para manter ou serem credenciados pelo Ministério da Agricultura, Pecuária e Abastecimento – MAPA. Posteriormente, a IN 51 de 2003 estabeleceu os requisitos da qualidade necessários para que o laboratório fosse credenciado ou reconhecido e, dentre outras exigências, deu o prazo de um ano para que fosse evidenciada a implantação do seu sistema da qualidade. Depois, a IN n° 01 de 16 de janeiro de 2007 acrescentou a necessidade de o laboratório comprovar a sua acreditação na Norma ABNT NBR ISO/IEC 17.025 – Requisitos Gerais para a Competência de Laboratórios de Ensaio e Calibração, através de documento emitido pelo INMETRO, para que pudesse integrar a RNLA.
Em 2010, o MAPA e o INMETRO firmaram Acordo de Cooperação Técnica (processo 21.000.004240/2007-38) com o objetivo de se apoiarem mutuamente, para o desenvolvimento da metrologia e da qualidade nas áreas da agropecuária e segurança dos alimentos, possibilitando o intercâmbio de informações técnico-científicas e de especialistas, formação e treinamento de recursos humanos, realização conjunta de programas de comparação interlaboratorial, acreditação de laboratórios de calibração e de ensaios, reconhecimento e monitoramento de instalações de teste segundo os Princípios das Boas Práticas de Laboratório-BPL e realização conjunta de programas de apoio a pesquisas para o desenvolvimento tecnológico.
A partir da publicação da IN n° 34 de 14 de julho de 2011, o MAPA determinou o prazo de até 36 meses para que os laboratórios credenciados apresentassem comprovante de acreditação junto ao INMETRO na Norma ABNT NBR ISO IEC 17.025, válido e atualizado, para todas as determinações analíticas ou ensaios. Este prazo, 14 de junho de 2014, coincidiria com o início da olimpíada que ocorreria no Rio de Janeiro.
A partir do 38° Congresso Brasileiro de Medicina Veterinária (CONBRAVET), realizado em Florianópolis em novembro de 2011, houve uma série de discussões sobre o tema de acreditação de laboratórios da área de saúde animal para fins de credenciamento no MAPA, capitaneadas pela médica veterinária Luciaurea Oliveira Cavalcanti com a valiosa cooperação de fiscais agropecuários federais e estaduais, além de alguns docentes. A princípio, notou-se grande resistência por parte da classe veterinária, mas com o passar do tempo a nova realidade foi se impondo e o tema foi se tornando mais aceito. Este fato se estendeu para os próximos congressos, o que permitiu uma difusão e popularização do tema, especialmente entre os envolvidos com a atividade laboratorial.
Publicada em 11 de dezembro de 2013, a IN n° 57 estabeleceu que o credenciamento e reconhecimento de laboratórios credenciados até o momento com base nos critérios anteriores, teriam prazo de validade máxima até 30 de junho de 2014. Vencido este prazo, houve o descredenciamento geral no Brasil, o que provocou transtornos irreparáveis em algumas empresas e pessoas ligadas ao setor. Foi um verdadeiro apagão no serviço de diagnóstico laboratorial no país no que diz respeito aos ensaios credenciados pelo Ministério. Esse momento foi de muito alvoroço, fato que, certamente, motivou a publicação da IN n° 19 de 25 de junho de 2014, poucos dias antes de expirar o prazo para apresentação do certificado de acreditação pelos laboratórios. Através desta IN, o MAPA ampliou esse prazo para 24 meses, contados a partir da solicitação de acreditação junto à CGCRE/INMETRO, a qual poderia ser feita até dezembro de 2014, para que os laboratórios credenciados apresentassem o seu certificado. Ou seja: agora seria possível entregar tal documento até dezembro de 2016. A figura 1 ilustra a sequência de normas publicadas e outros eventos que abordam a qualidade do diagnóstico laboratorial relacionados aos serviços de defesa agropecuária nos últimos anos no Brasil.
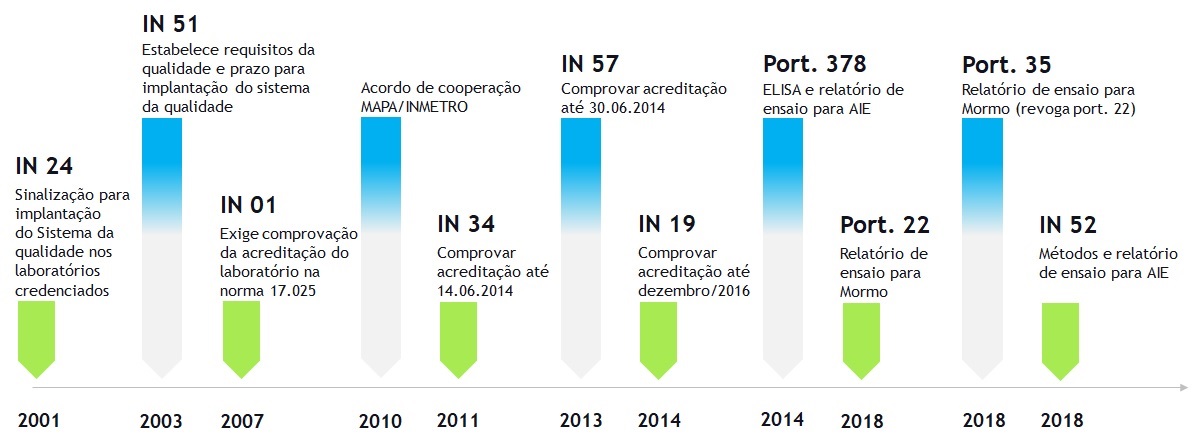
Linha do tempo das publicações do MAPA e eventos que fazem referência à qualidade em laboratórios agropecuários entre 2001 e 2018.
Aparentemente, o que se percebe de toda essa movimentação é que há uma boa intenção de melhorar a qualidade do diagnóstico no Brasil, mas há também uma fragilidade nas legislações produzidas, fragilidade essa percebida pela quantidade de portarias e instruções normativas pouco abrangentes, outras que tratam dos mesmos temas já consolidados em legislações anteriores e também algumas que abordam os mesmos assuntos com pequenas variações, em curtos intervalos de tempo.
A vulnerabilidade nas legislações é percebida também em relação aos programas específicos. Para ficar apenas em um exemplo, mencionam-se as últimas publicações sobre o Programa Nacional de Sanidade dos Equídeos-PNSE. A Portaria 378 de 17 de dezembro de 2014 que modifica o anexo da portaria 84 de 1992 trata, dentre outros assuntos, da necessidade de emissão dos resultados dos exames de Anemia Infecciosa Equina em um documento denominado Relatório de Ensaio para atender a norma 17.025. Somente em março de 2018, a Portaria 22 foi tratar do Relatório de Ensaio para o exame de Mormo. Esta portaria, por sua vez, durou apenas um mês, pois foi revogada pela Portaria 35 de 17 de abril de 2018, a qual apresentou pequeníssimas alterações em relação ao texto publicado anteriormente. Em 27/11/2018 foi publicada mais uma instrução sobre AIE, a IN 52 que define os requisitos e critérios para a realização do diagnóstico dessa doença por meio das técnicas Imunodifusão em Gel de Agar (IDGA) e ensaio imunoenzimático (ELISA – Enzyme-Linked Immunosorbent Assay), além de detalhar os itens que devem constar no relatório de ensaio, temas já tratados de forma mais superficial pela portaria 378/2014.
Outro aspecto que certamente pode impactar a qualidade do diagnóstico no nosso país é a variedade de políticas ou ações diferentes para cada programa sanitário. Menciona-se o Programa Nacional de Controle e Erradicação da Brucelose e Tuberculose-PNCEBT, no qual os exames de brucelose são realizados por dois entes juridicamente distintos e com níveis de exigência, pelo menos aparentemente, bem diferentes. De um lado estão os laboratórios credenciados pelo MAPA, portanto acreditados pela CGCRE/INMETRO, que são avaliados frequentemente, fazem ensaios de proficiência e outros mecanismos para comprovar sua competência, enquanto do outro lado estão os profissionais habilitados que fazem os mesmos exames de triagem para diagnóstico dessa importante enfermidade, porém não precisam ser credenciados para essa tarefa, o que pode, portanto, comprometer a qualidade desse diagnóstico.
Apresenta-se a seguir alguns aspectos importantes para a melhoria da qualidade do diagnóstico na área de saúde animal no Brasil:
- Ouvir os envolvidos no processo do diagnóstico laboratorial. Há, além dos cientistas e acadêmicos, pessoas capacitadas nos laboratórios públicos e privados que podem sugerir melhorias nas legislações através de uma consulta pública ou outro mecanismo participativo;
- Ampliar a abrangência das instruções normativas e portarias que regulamentam os programas sanitários. Os instrumentos legais devem abranger as enfermidades atualmente controladas pelos programas e, se possível, apresentar uma abrangência tal que as futuras doenças que, porventura venham a ser controladas, já possam ser contempladas na legislação. No que diz respeito ao diagnóstico, as normas devem ser mais amplas, porém com especificidade suficiente para garantir a qualidade e a padronização dos ensaios, métodos e relatórios;
- Os modelos de formulários. Neste sentido, segue-se com a sugestão anterior de abrangência. Mais uma vez, tomando o PNSE como exemplo, e apenas como exemplo, fala-se sobre as requisições. Atualmente, o médico veterinário requisitante deve preencher um formulário para solicitar exame de AIE e outro para Mormo, quando o recomendável seria uma única requisição para essas duas e tantas outras enfermidades que o MAPA vier a controlar no país. A figura 2 mostra um modelo possível de requisição para o programa como um todo. Este mesmo raciocínio pode ser aplicado a outros programas sanitários, tais como Programa Nacional de Sanidade Avícola-PNSA, Programa Nacional de Sanidade Suídea-PNSS, Programa Nacional de Controle e Erradicação da Brucelose e Tuberculose-PNCEBT, dentre outros.
- Requisições. O preenchimento manuscrito de requisições é um fator que pode comprometer a qualidade dos exames, no que diz respeito à clareza das informações. Já existem mecanismos tecnológicos suficientes para tornar a requisição mais interativa entre laboratórios e requisitantes. Considerando-se que os requisitantes são responsáveis legais pelos dados informados, deveriam ser passíveis de fiscalização por parte dos órgãos de defesa agropecuária. Para tanto, deveriam manter uma via da requisição arquivada;
- Deve-se avançar na disponibilização on-line dos resultados dos exames. Este é um aspecto que facilita bastante a logística de envio dos relatórios de ensaio, reduz custos operacionais e ainda aumenta a segurança para o sistema de defesa sanitária, diminuindo a possibilidade de fraudes. O fiscal agropecuário, o responsável técnico por eventos ou por estabelecimentos ou o barreirista poderia, a qualquer momento, consultar se aquele exame foi realmente feito pelo laboratório indicado. Esta já é uma prática consolidada para outros exames no Brasil.

Modelo de requisição de exames para várias doenças controladas por um mesmo programa sanitário.
- A comunicação de resultados diferentes de negativo deveria ser feita também aos requisitantes e proprietários. Desta maneira, os mesmos já estariam, de alguma forma, sendo notificados e poderiam ser convocados a colaborar com a localização e entrega do animal para as devidas medidas sanitárias a serem adotadas.
Entende-se que, passada a primeira e importante fase de acreditação dos laboratórios, com um nivelamento e padronização dos procedimentos em todo o país, com a regularidade das avaliações realizadas a cada dois anos pela CGCRE/INMETRO, chegou a hora de avançar um pouco mais, especialmente agora, com a publicação da versão 2017 da norma 17.025, que dá uma maior liberdade aos laboratórios na implementação dos seus procedimentos internos, desde que façam as devidas análises dos riscos.


